Las baterías y acumuladores son elementos esenciales en nuestro día a día, impulsando desde nuestros teléfonos móviles hasta los vehículos eléctricos. Su funcionamiento, sin embargo, puede resultar complejo para muchos. En esta guía completa, desentrañaremos los secretos de estos dispositivos, explorando sus componentes, su funcionamiento interno y las diferencias entre baterías y acumuladores.
- Puntos Clave
- El concepto de acumulador: ¿Qué es y cómo funciona?
- El proceso de generación de corriente: Oxidación y reducción
- Tipos de acumuladores: Baterías y pilas
- Tipos de baterías: Una clasificación basada en su composición
- Recarga de acumuladores: Inversión del proceso químico
- La terminología actual: Pila vs. Batería
- Video sobre Funcionamiento de Baterías y Acumuladores: Guía Completa
- Preguntas Frecuentes
- Resumen Final
- Compartelo
Puntos Clave
- Las baterías almacenan energía química que se convierte en energía eléctrica.
- Los acumuladores, tipo de batería, son recargables y almacenan energía eléctrica.
- Las baterías se componen de ánodo, cátodo, electrolito y separador.
- El ánodo libera electrones durante la descarga, y el cátodo los recibe.
- El electrolito permite el flujo de iones entre el ánodo y el cátodo.
- La reacción química en la batería genera corriente eléctrica.
- Los acumuladores se recargan mediante la aplicación de corriente eléctrica externa.
- La energía almacenada en una batería se mide en Amperios-hora (Ah).
El concepto de acumulador: ¿Qué es y cómo funciona?
Definición de acumulador: Almacenamiento de energía electroquímica
Un acumulador, también conocido como batería o acumulador de corriente, es un dispositivo que almacena energía química y la convierte en energía eléctrica. El proceso fundamental es el almacenamiento de energía mediante una reacción química reversible, que luego se libera en forma de corriente eléctrica. Para entender el funcionamiento de un acumulador, hay que entender que se basa en un proceso electroquímico donde la energía se almacena en forma de energía potencial química, la cual se libera como energía eléctrica cuando se necesita. En otras palabras, un acumulador transforma la energía química en energía eléctrica, y la energía eléctrica en energía química.
Imaginate que la energía química almacenada en el acumulador es como la energía potencial de un objeto situado a cierta altura. Al caer, esta energía potencial se convierte en energía cinética, que es la energía del movimiento. En el acumulador, la energía química se libera como energía eléctrica, que puede utilizarse para alimentar dispositivos o realizar tareas.
Componentes clave de un acumulador: La celda electroquímica
La base fundamental de cualquier acumulador es la celda electroquímica, que es una unidad básica de almacenamiento de energía que consiste en dos electrodos metálicos sumergidos en un electrolito líquido. La interacción entre estos tres componentes produce una diferencia de potencial (d.d.p.) entre los electrodos, la cual es la base para la generación de corriente eléctrica.
Los electrodos: Ánodo y cátodo
Los electrodos son los elementos clave en la celda electroquímica. Son dos placas conductoras de la electricidad, generalmente metálicas, que se encuentran sumergidas en el electrolito. Se diferencian por su función en el proceso electroquímico:
- Ánodo: Es el electrodo donde se produce la oxidación. En este proceso, el ánodo pierde electrones y se convierte en iones positivos que se liberan al electrolito.
- Cátodo: Es el electrodo donde se produce la reducción. En este proceso, el cátodo gana electrones y se convierte en iones negativos que también se liberan al electrolito.
La diferencia de potencial entre el ánodo y el cátodo es lo que impulsa el flujo de corriente eléctrica.
El electrolito: Conductividad y reacciones químicas
El electrolito es una solución conductora de electricidad que se encuentra entre los electrodos. Permite el movimiento de los iones entre los electrodos, lo que es fundamental para el funcionamiento de la celda.
El electrolito puede ser líquido, sólido o incluso un gel. La composición química del electrolito juega un papel crucial en el tipo de reacción electroquímica que se produce en la celda y en la energía que se almacena.
La interacción del electrolito con los electrodos crea reacciones de oxidación y reducción, que son las que liberan o almacenan energía.
El proceso de generación de corriente: Oxidación y reducción
Cuando se conecta una carga a un acumulador, se crea un circuito cerrado que permite el flujo de corriente eléctrica. Este flujo de corriente está impulsado por la diferencia de potencial (d.d.p.) entre los electrodos.
Lee También Pilas: Tipos, Características y Guía de Compra
Pilas: Tipos, Características y Guía de CompraEl flujo de electrones: Del cátodo al ánodo
La d.d.p. se genera debido a la diferencia en el potencial electroquímico entre el ánodo y el cátodo. Esto se debe a las reacciones de oxidación y reducción que se producen en los electrodos. La energía química almacenada en el acumulador se libera en forma de corriente eléctrica, que circula del cátodo al ánodo a través del circuito externo.
La diferencia de potencial: Fuente de la corriente eléctrica
La d.d.p. entre los electrodos es la fuerza motriz que impulsa la corriente eléctrica. Esta fuerza se mide en voltios (V), y una d.d.p. mayor significa una mayor fuerza impulsora para la corriente.
Tipos de acumuladores: Baterías y pilas
Existen dos tipos principales de acumuladores: baterías y pilas:
Baterías: Unión de celdas electroquímicas en serie
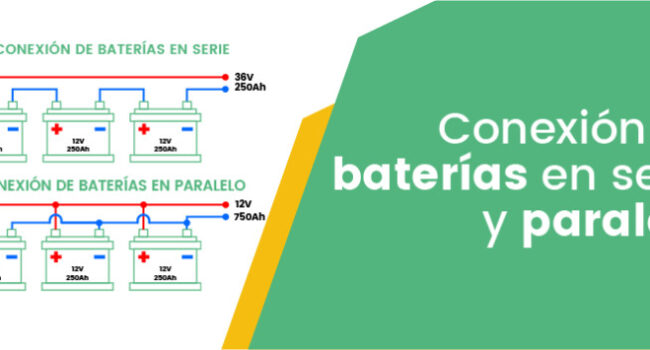
Las baterías se componen de varias celdas electroquímicas conectadas en serie, lo que significa que los polos positivos de las celdas se conectan a los polos negativos de las siguientes celdas. La unión en serie de las celdas permite aumentar la tensión total de la batería, es decir, la diferencia de potencial (d.d.p.) entre sus terminales.
Un ejemplo común son las baterías de los automóviles, que típicamente tienen 12 voltios, formados por seis celdas electroquímicas conectadas en serie, cada una con una d.d.p. de 2 voltios.
Pilas: Una única celda electroquímica
Las pilas son acumuladores que se basan en una única celda electroquímica. Tienen una tensión menor que las baterías, pero su tamaño es más reducido y su peso es menor.
Las pilas se usan generalmente en dispositivos de bajo consumo energético, como los controles remotos, las calculadoras o los relojes.
Tipos de baterías: Una clasificación basada en su composición
Las baterías se clasifican según el tipo de materiales que componen la celda electroquímica. Entre los tipos más comunes se encuentran:
Baterías de plomo-ácido: Tecnología tradicional
Las baterías de plomo-ácido son las más antiguas y las más usadas en automóviles. Se caracterizan por su bajo costo y su alta capacidad de almacenamiento de energía. Su electrolito es una solución acuosa de ácido sulfúrico, y los electrodos son de plomo y óxido de plomo.
Baterías de litio: Mayor densidad energética
Las baterías de litio son más modernas y se caracterizan por su mayor densidad energética. Esto significa que almacenan más energía en un volumen dado. Son más ligeras y compactas, lo que las hace ideales para dispositivos portátiles, como los teléfonos móviles o los ordenadores portátiles.
Lee También Cargador de Batería por Goteo: Carga Segura y Eficiente para Larga Duración
Cargador de Batería por Goteo: Carga Segura y Eficiente para Larga DuraciónLas baterías de litio se basan en el uso de litio metálico como ánodo, y diferentes compuestos de litio como cátodo. El electrolito es una solución orgánica que contiene sales de litio.
Recarga de acumuladores: Inversión del proceso químico
Una de las características más importantes de los acumuladores es su capacidad de recarga. La recarga consiste en invertir el proceso químico interno del acumulador, restaurando su d.d.p. original.
Baterías recargables: Recuperando la d.d.p.
Las baterías recargables, también conocidas como baterías de acumuladores, permiten que el proceso químico interno se revierta aplicando una corriente eléctrica externa. Esta corriente invierte la reacción química, restaurando la d.d.p. original.
Las baterías recargables se utilizan en aplicaciones donde la energía se necesita de manera repetida, como en los automóviles, los ordenadores portátiles, los teléfonos móviles y los vehículos eléctricos.
Baterías no recargables: Ciclo de vida limitado
Las baterías no recargables, como las pilas convencionales, tienen un ciclo de vida limitado. Esto significa que solo pueden descargarse una vez y luego deben ser reemplazadas. Una vez agotada la energía química almacenada, ya no pueden utilizarse.
La energía química almacenada en estas baterías se libera en una reacción química irreversible, por lo que no es posible invertir el proceso y restaurar su d.d.p. original.
La terminología actual: Pila vs. Batería
Históricamente, la terminología ha evolucionado, y en la actualidad se usan tanto "pila" como "batería" para referirse a acumuladores, aunque con una ligera diferencia:
Evolución histórica: Distinción actual
En la actualidad, "pila" se utiliza generalmente para referirse a acumuladores no recargables, mientras que "batería" se utiliza para acumuladores recargables.
Uso coloquial: Pila para dispositivos pequeños, batería para sistemas mayores
En el lenguaje coloquial, se suele usar "pila" para referirse a los acumuladores pequeños, como las que se usan en los controles remotos, las calculadoras, los relojes o los juguetes. Por otro lado, se suele utilizar "batería" para referirse a acumuladores más grandes, como las que se usan en los automóviles, los ordenadores portátiles, los teléfonos móviles o los vehículos eléctricos.
la terminología actual es un poco confusa, pero es importante entender que "pila" se utiliza para referirse a los acumuladores que no se pueden recargar, mientras que "batería" se utiliza para referirse a los acumuladores que sí se pueden recargar.
Lee También Cargador 1.5 Amperios: Carga Rápida y Segura para Tus Dispositivos
Cargador 1.5 Amperios: Carga Rápida y Segura para Tus DispositivosVideo sobre Funcionamiento de Baterías y Acumuladores: Guía Completa
Preguntas Frecuentes
¿Cuál es la diferencia entre una batería y un acumulador?
En la actualidad, los términos "batería" y "acumulador" se utilizan casi como sinónimos. Sin embargo, existe una diferencia sutil: una batería se compone de varias celdas electroquímicas conectadas en serie, mientras que un acumulador es una única celda electroquímica. Por ejemplo, una batería de coche de 12 voltios tiene seis celdas de 2 voltios cada una. En el lenguaje coloquial, se suele usar "batería" para acumuladores grandes y "pila" para los más pequeños, pero la distinción principal radica en la capacidad de recarga.
¿Cómo se recarga una batería?
La recarga de una batería implica invertir el proceso químico que libera la energía. Una corriente eléctrica externa se aplica al acumulador, forzando la inversión del flujo de electrones y la reconstrucción de los compuestos químicos en los electrodos. Este proceso restaura la energía química almacenada y, por lo tanto, la diferencia de potencial (d.d.p.) entre los terminales de la batería.
¿Cuál es la diferencia entre una batería de plomo-ácido y una batería de litio?
Las baterías de plomo-ácido son las más tradicionales y se caracterizan por su bajo costo y alta capacidad de almacenamiento de energía. Sin embargo, son pesadas y tienen una vida útil limitada. Las baterías de litio, por otro lado, son más ligeras, compactas y tienen una mayor densidad energética, lo que significa que almacenan más energía en un volumen dado. Su vida útil también es mayor que las de plomo-ácido, pero son más costosas.
¿Qué es el electrolito y por qué es importante?
El electrolito es una solución conductora de electricidad que se encuentra entre los electrodos de la batería. Su función principal es permitir el movimiento de iones entre los electrodos, lo que es crucial para el flujo de corriente eléctrica. La composición química del electrolito determina el tipo de reacciones químicas que se producen en la batería y, por lo tanto, la cantidad de energía que se puede almacenar.
¿Cómo se determina la capacidad de una batería?
La capacidad de una batería se mide en amperios-hora (Ah) y representa la cantidad de corriente eléctrica que puede entregar durante una hora. Una batería con una mayor capacidad puede proporcionar una mayor cantidad de corriente durante un tiempo más largo. La capacidad de una batería también se puede expresar en miliamperios-hora (mAh), especialmente para baterías pequeñas.
Resumen Final
En este recorrido por el mundo de los acumuladores, hemos desentrañado los misterios de su funcionamiento, desde la celda electroquímica que los compone hasta los diferentes tipos de baterías y pilas que existen. Hemos visto cómo la interacción entre los electrodos y el electrolito genera energía eléctrica mediante reacciones químicas reversibles, permitiendo almacenar y liberar energía de manera eficiente. De este viaje podemos extraer una reflexión: la tecnología de los acumuladores avanza constantemente, ofreciéndonos soluciones cada vez más eficientes y sostenibles para alimentar nuestro mundo.
Compartelo
¿Quieres entender cómo funcionan las baterías y los acumuladores? ¡Esta guía completa te lo explica todo! Desde la electroquímica hasta los distintos tipos de baterías, este texto te ayudará a comprender el funcionamiento de estos dispositivos esenciales en nuestra vida diaria. ¡Comparte este conocimiento con tus amigos y familiares y desvela los secretos de la energía!
Deja una respuesta





También te puede interesar: